随着我国临床诊断需求的不断增长,以及研发技术的不断提高,体外诊断(IVD)行业已经成为我国医药行业中发展最快,也最活跃的细分行业之一。虽然目前我国体外诊断行业尚处于发展初期,但其发展一直受国家产业政策重点支持。“十一五”期间,国家“863”计划首次支持了生物医学关键试剂的重点项目,2005年以来,政府相关部门更是相继出台了多项政策,将体外诊断试剂、诊断仪器、诊断相关酶制剂等产业的发展列为重点发展项目,将体外诊断列为战略性新兴产业。
体外诊断行业包括仪器、试剂和耗材,其中IVD市场80%是试剂,本报告以诊断试剂为主,兼顾部分耗材情况,较少讨论诊断仪器。
1.体外诊断试剂概况
体外诊断,即In Vitro Diagnosis,缩写IVD,这是一个宽泛的概念,指在人体之外,通过对人体的样品(血液、体液、组织等)进行检测而获取临床诊断信息的产品和服务,包括试剂、试剂产品、校准材料、控制材料、成套工具、仪表、装置、设备或系统等等,包括血液检测、尿液检测等等。本报告以体外诊断试剂为核心,并兼顾部分耗材情况,探讨这个行业的发展趋势和投资机会。
1.1 体外诊断试剂是什么
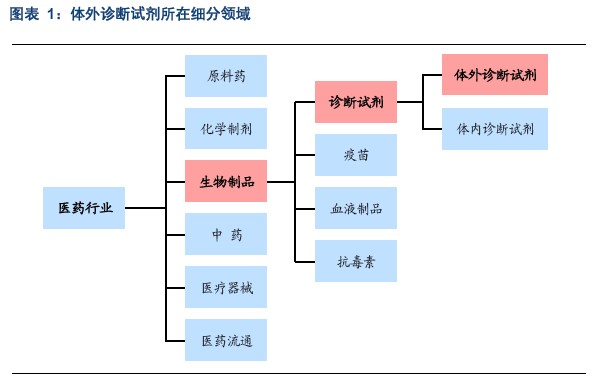
体外诊断试剂隶属于生物制品行业,是下属诊断试剂行业中的一个细分领域。
体外诊断试剂是指用于单独使用或与仪器、器具、设备或系统组合使用,在疾病的预防、诊断、治疗监测、预后观察、健康状态评价以及遗传性疾病的预测过程中,用于对人体样本(各种体液、细胞、组织样本等)进行体外检测的试剂、试剂盒、校准品(物)、质控品(物)等,其作用原理为:诊断试剂与体内物质在体外发生生物化学反应,体液内某些物质——比如糖、脂肪和蛋白质——会和体外诊断试剂在特定条件下发生特定的反应,生成特定的产物,消耗定量的体外诊断试剂,而这些是可以被定性或者定量测量出来的,再通过与正常值的对比,从而判断检测对象的生理状态是否正常。
1.2 体外诊断试剂分类
体外诊断试剂的分类方法比较多,通常的分类方法有以下几种:
第一,按照检测原理分类,这也是现在的主流分类方法。根据检测原理或者检测方法,体外诊断试剂可以分为生化诊断试剂、免疫诊断试剂、分子诊断试剂、微生物诊断试剂、尿液诊断试剂、凝血类诊断试剂、血液学和流式细胞诊断试剂等,生化、免疫和分子诊断试剂为我国诊断试剂主要的三大类品种,目前分子诊断中的核酸诊断占据主要市场,生物芯片是未来发展的重要趋势,但目前由于成本较高,开发难度大,使用量还比较小。

对于以上三种分类,如果从检测端角度来看,其中生化诊断检测项目的检测原理基本相同,主要是利用某些特定的生物化学反应的特定底物或者产物,然后再通过检测仪器(如分光光度计)定量检测出标的物浓度,从而推算出人体的某些生化指标,如糖、脂肪和蛋白质含量是否在正常范围内。
免疫诊断在原理上是利用抗原抗体的特异性结合,但是检测端的方法就比较多了,检测方式多样化,比如利用放射性元素的放射性而准确测量抗原抗体结合的放射免疫(放免)、利用氯金酸在特定环境下通过静电作用与蛋白质大分子结合的胶体金技术、利用活性酶作为标记物的酶联免疫(酶免)、利用镧系元素(稀土元素)螯合物荧光寿命长的特定进行检测的时间分辨荧光法(TRFIA)和利用化学发光原理和免疫反应原理相结合的化学发光检测(CLIA)。
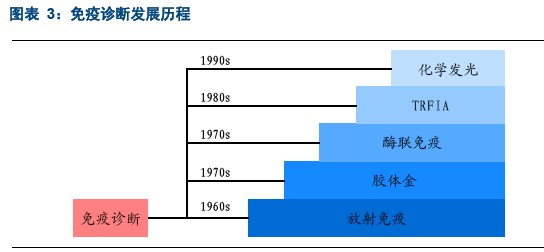
放免由于对环境污染较大,现在逐渐被其他免疫诊断方法所替代,目前酶免是免疫诊断中比较主流的方法。
核酸诊断是目前分子诊断中的主要部分,另一种是生物芯片技术。分子诊断的检测目标直接是决定生命性状的遗传物质和表现形式,包括DNA、RNA和蛋白质。在具体诊断技术方面,核酸诊断中的代表技术是聚合酶链式反应(PCR),此外还有NDA测序、荧光原位杂交技术(FISH)、DNA印迹技术(DNA blotting)、单核苷酸多态性(SNP)和连接酶链反应(LCR)。生物芯片包括基因芯片和蛋白质芯片等。目前PCR是核酸检测中主要使用的方法。

第二,按医疗器械受理和审评的体外诊断试剂,它包括临床血液学和体液学检验试剂、临床化学检验试剂、临床免疫学检验试剂和微生物学检验试剂等共计九种。
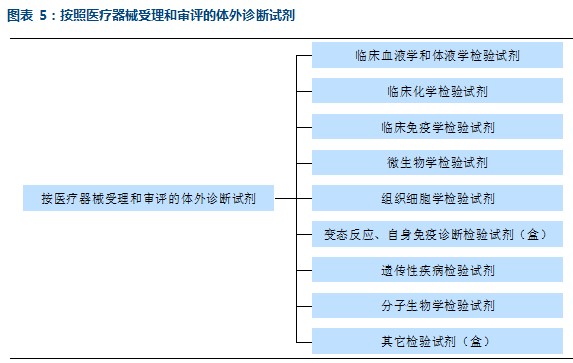
需要特别指出的是按照医疗器械生产监督管理办法管理的体外诊断试剂,不包括国家法定用于血源筛查和采用放射性核素标记的体外诊断试剂产品。
第三,按药品受理和审评的体外诊断试剂。按照这一分类原则,可将体外诊断试剂分为六大类,包括ABO血型定型试剂(盒)、乙型肝炎表面抗原(HBsAg)试剂(盒)、丙型肝炎病毒(HCV)抗体试剂(盒)、人类免疫缺陷病毒HIV(1+2型)抗体试剂(盒)、人类免疫缺陷病毒抗原/抗体诊断试剂(盒)、梅毒螺旋体抗体试剂(盒)和放射免疫检测试剂(盒)。
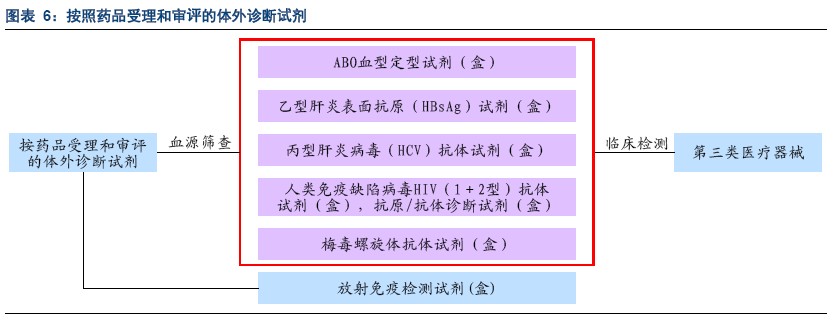
除放免试剂(盒)外,前五种诊断试剂如果用于血源筛查时,按照药品受理和审评;如果用于临床诊断,按照第三类医疗器械进行管理。前五种诊断试剂如果用于血源筛查则需要进行批批检,以保障临床用血的安全。
第四,按照《体外诊断试剂注册管理办法》分类,根据产品风险程度由高至低的顺序,将按照医疗器械进行管理的体外诊断试剂依次分为第三类、第二类、第一类产品,并实施分类注册管理,其中第三类产品注册管理部门为国家食品药品监督管理局,第二类产品为省、自治区、直辖市药品监督管理部门,第一类产品为设区的市级药品监督管理机构。

(一)第三类产品:国家药监局直接管理
1.与致病性病原体抗原、抗体以及核酸等检测相关的试剂;
2.与血型、组织配型相关的试剂;
3.与人类基因检测相关的试剂;
4.与遗传性疾病相关的试剂;
5.与麻醉药品、精神药品、医疗用毒性药品检测相关的试剂;
6.与治疗药物作用靶点检测相关的试剂;
7.与肿瘤标志物检测相关的试剂;
8.与变态反应(过敏原)相关的试剂。
(二)第二类产品:各省、自治区、直辖市级药监局管理
1.用于蛋白质检测的试剂;
2.用于糖类检测的试剂;
3.用于激素检测的试剂;
4.用于酶类检测的试剂;
5.用于酯类检测的试剂;
6.用于维生素检测的试剂;
7.用于无机离子检测的试剂;
8.用于药物及药物代谢物检测的试剂;
9.用于自身抗体检测的试剂;
10.用于微生物鉴别或药敏试验的试剂;
11.用于其他生理、生化或免疫功能指标检测的试剂。
(三)第一类产品:市级药监局管理
1.微生物培养基(不用于微生物鉴别和药敏试验);
2.样本处理用产品,如溶血剂、稀释液、染色液等。
2.体外诊断试剂产业链情况
体外诊断试剂上游的核心原料包括诊断酶、引物、抗原、抗体等等,此外还有各种精细化学原料,包括氯化钠、碳酸钠和各种氨基酸以及有机酸等,这些精细化工品的作用主要是调配诊断试剂的缓冲溶液系统。体外诊断试剂的下游主要是医疗和科研机构,按照用途可以大致划分为医学检测和血源筛查两块。和体外诊断试剂相关的两个平行的行业包括体外诊断仪器和体外诊断耗材两部分。
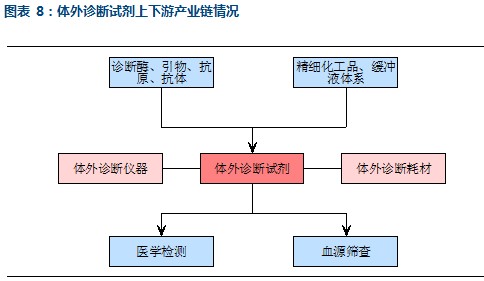
2.1 体外诊断仪器情况
体外诊断仪器目前以进口产品居多,尤其是中高端市场这一块,国外设备占据了主要市场份额。不同类型的体外诊断试剂对仪器的依赖度也不同,例如生化诊断仪器以开放式居多,免疫诊断仪器以封闭式居多。此外,同种类型的体外诊断仪器自动化程度不同,对于试剂的开放程度也不相同,通常高度自动化的仪器是封闭式的,自动化程度较低的仪器是开放式的。
以生化检测设备为例,生化分析仪是临床生化诊断的主要诊断仪器,也是大多数医院最基本的和必备的检验设备。与手工、半自动生化分析仪相比,全自动生化分析仪具有操作简便、检测速度快、精密度高、重复性好、检测结果不受操作影响等优势,是生化检测发展的方向。发达国家大部分生化诊断均已实现自动化,我国由于经济发展水平的差异,全自动生化分析仪在二三级医院高端市场中使用较多,基层医院还处于手工、半自动与全自动生化分析仪并存的时期
在我国的全自动生化分析仪市场中,日立、奥林巴斯、贝克曼(奥林巴斯诊断业务被贝克曼收购)三家公司占据了约60-70%的市场份额,其中日立占有约30-40%的市场份额。生化试剂主要用于配合手工、半自动和全自动生化分析仪等检验设备使用。
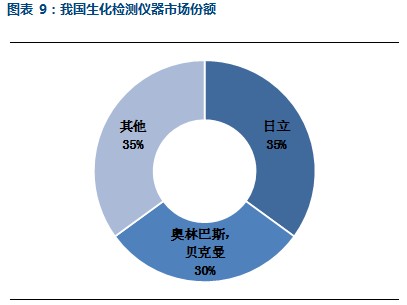
2.2 体外诊断耗材情况
体外诊断耗材主要指真空采血管,由于静脉血液所含有的丰富病理信息,临床检验实验室常用标本中70%是人体静脉血液标本,真空采血管作为主要的体外诊断样本容器,在诊断过程中起着至关重要的作用。
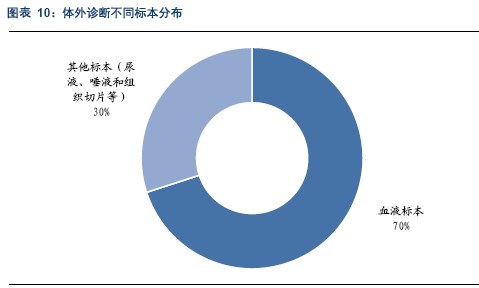
目前真空采血已经发展到第三代,是循证医学发展的产物。最早的采血管是开放式,很容易受到外部环境的污染,第一代真空采血管采用负压技术,使得整个采血过程与外界隔离,第一代真空采血管的出现是传统采血方式的革命性事件。在第一代真空采血管的基础上,第二代产品在血液样本采集、盛装和转运环节制定了标准化和规范化流程,使得真空采血管的规格、材质、抽吸量、添加剂等关键指标有了国际标准。第三代真空采血系统考虑到了血液样本离开人体后的变异作用,这样的变异作用将对检测结果造成影响,所以这一代真空采血管的作用已由静脉血液标本的采集和转运装置转变为静脉血液标本分析前变异控制和处理系统。
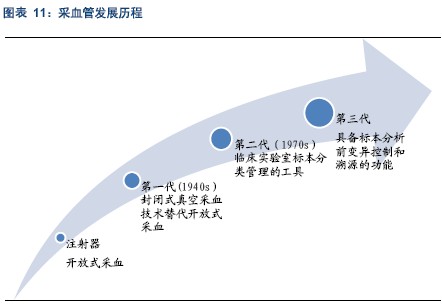
采血管是血液离开人体后的第一站,血液离开人体过程中和离开人体后,由于活细胞与活性蛋白对环境的变化发生应激反应,致使血液标本的物理性质、化学性质、生物学性质、生理学性质等发生变化,改变其原始性状,是血液检测面临的主要问题。血液标本发生变异导致检验结果无法确切地说明在体组织与器官之间的真实情况,医疗机构的检验结果可能是一个失真信息的报告,从而违背了循证医学追求的目标。所以针对不同的血液检测项目,要使用不同的真空采血管。在具体实践中,某些诊断项目,不同的诊断试剂对真空采血管的要求也不同,某些诊断试剂的诊断结果会受到采血管的显著影响。
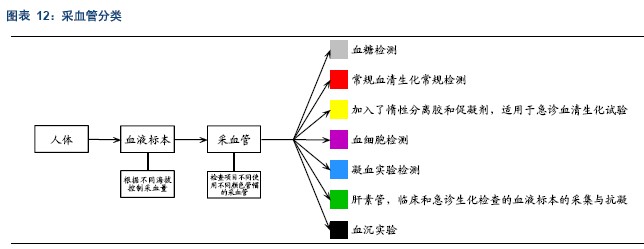
2.3 下游需求情况
体外诊断试剂和仪器的下游需求端可以分为两类,一类是用于医学检测,包括医院、体检中心、独立实验室以及防疫站,其中医院是体外诊断行业最大的下游需求端;第二类是用于血源筛查,这个领域的需求端主要是血站系统,其使用总量相对较小,但是对于诊断试剂有着较高的灵敏度的要求。
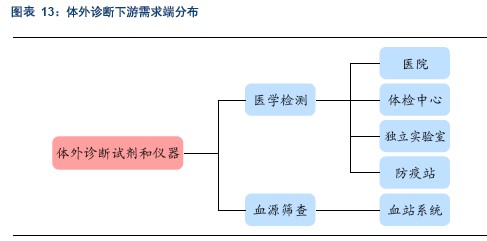
单从使用量上来看,血站系统在体外诊断试剂市场中占比较低,从检测项目上来看,血站系统的检测项目相对较窄,但是从诊断试剂的使用结构上来看,目前血源筛查主要使用的免疫诊断试剂中的酶联免疫试剂,同时目前在推广核酸诊断,而在医院市场中,核酸诊断的使用则相对较少,所以血站系统的体外诊断试剂使用量虽然比较小,但是对于某些特定的诊断试剂的需求量相对比较大。
3.体外诊断试剂市场分析
3.1 我国体外诊断试剂行业现状
体外诊断市场中包括诊断试剂、耗材和仪器设备三部分,其中诊断试剂是占比最大的一块,比例在80%左右,其余20%左右的市场是诊断设备和耗材。2011年,我国体外诊断市场的总规模预计在146亿元左右,从2007年至2010年,我国体外诊断市场整体增速平稳上升。预计在2014年体外诊断市场总体规模将超过260亿元,2010-2014年的年均复合增速在21.6%左右。
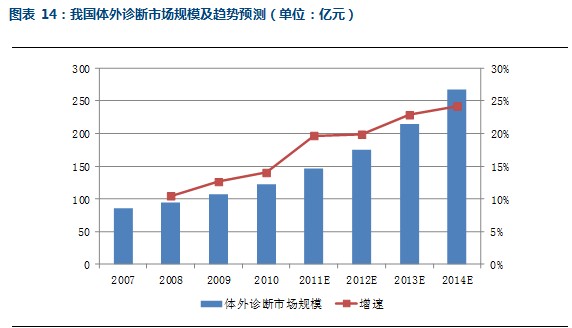
体外诊断领域中,诊断试剂占比在80%以上,根据预测,2011年我国体外诊断行业将近150亿元的市场规模中,体外诊断试剂的规模为120亿元左右,占比82%,其中免疫诊断试剂占整个诊断试剂市场的约29%,生化诊断试剂占26%,免疫诊断和生化诊断主要用于临床诊断,二者占全部诊断试剂市场份额的55-60%的份额;包括分子诊断试剂在内的其他诊断试剂占比27%
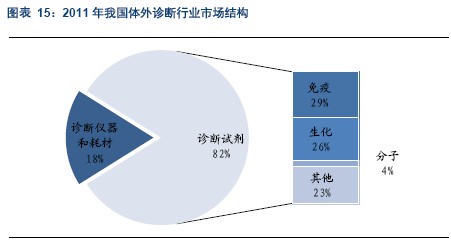
体外诊断领域中,诊断试剂占比在80%以上,根据预测,2011年我国体外诊断行业将近150亿元的市场规模中,体外诊断试剂的规模为120亿元左右,占比82%,其中免疫诊断试剂占整个诊断试剂市场的约29%,生化诊断试剂占26%,包括分子诊断试剂在内的其他诊断试剂占比27%。
2010年我国体外诊断试剂的市场规模将近100亿元,预计2014年这一数据将接近230亿元,4年间的复合增速约为23.1%,略高于体外诊断行业的整体增速。
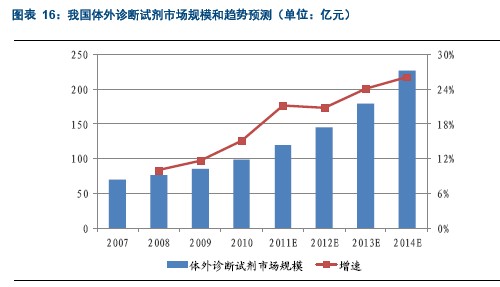
3.2 全球体外诊断试剂行业情况——核酸诊断异军突起
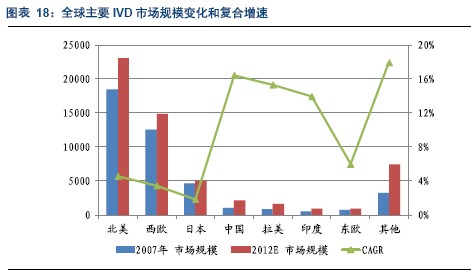
根据专业机构预测,2012年全球的IVD市场规模将超过560亿美元,2007年这一数字约为420亿美元,5年间的复合增速为6.07%。从全球的增速情况来看,IVD市场基本已经步入了成熟阶段。

从地区来看,全球不同地区和国家的IVD市场表现出了巨大的差异,北美、西欧和日本等发达国家和地区的IVD市场规模体量大,它们占据了全球约3/4的IVD市场规模,但是他们的市场已步入了成熟期,增速较慢,预计2007-2012年的年均复合增速在4%左右,而以中国、拉丁美洲和印度为代表的新型市场,虽然目前的市场总量较小,但是增速高,年均复合增速在12-16%之间,其中中国的IVD市场规模预计2012年将达到将近22亿美元(约合143亿人民币),在全球的市场份额将由2007年的2%上升到4%。
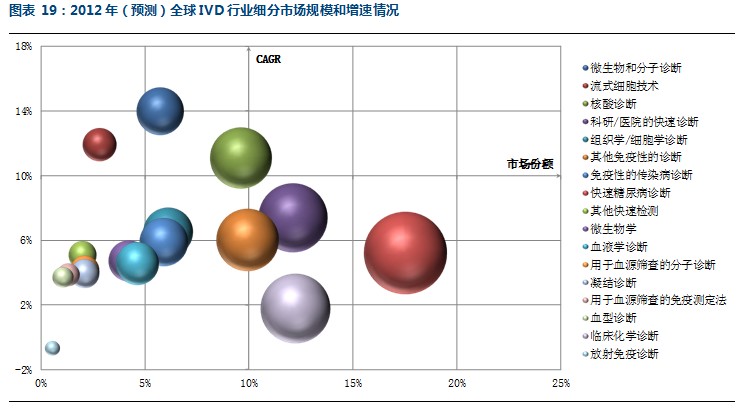
在具体品种方面,如下图所示,横轴为细分品种的市场份额(2012年预测),纵轴为2007-2012年的年均复合增速,球体大小代表细分市场规模的大小。图表中右侧图例是按照CAGR由高到底的顺序排列。我们以10%的市场份额和10%的复合增速为界,将图分为4个区域,我们注意到在IVD行业内没有体量大增速高的细分领域,微生物和分子诊断、流式细胞技术以及核酸诊断是增速最快的三个品种,它们的年均复合增速在10%以上,其中核酸诊断在全部细分领域中,是唯一一个兼顾了市场容量和复合增速的细分领域。
在市场规模方面,快速诊断试剂(POCT:Point of Care testing)占据了主要的市场份额,其中市场份额最大的是用于糖尿病快速诊断的试剂,以及用于科研和医院系统的快速诊断试剂,二者合计占据了30%的市场份额。此外,临床化学诊断试剂的市场份额12%,是第三大细分领域。这三个细分市场的特点是容量大,增速低,其复合增速在5%左右,临床化学诊断试剂的复合增速仅为2%左右。
4. 我国体外诊断试剂行业未来驱动因素
体外诊断试剂作为诊断用药,与一般治疗用药不同,诊断试剂是医生给患者提供诊断方案前的重要参考依据,我们认为诊断试剂行业的扩充将最直接受益于我国诊疗人次的提高和医疗水平的提升,就诊人次上升和卫生费用的提高将是带动行业发展的持久动力,而我国传染病形式的严峻、血源筛查核酸检测工作的推广和行业整合将是未来推动诊断试剂行业发展的直接动力。
4.1 诊疗人次稳步增长,卫生费用增长乏力,结构调整或成为扩容动力
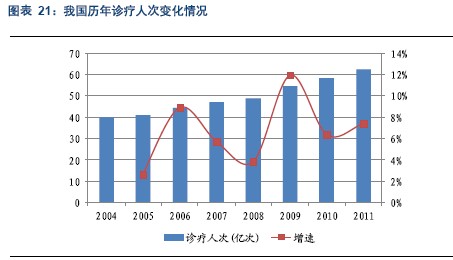
诊疗人次稳步增长是体外诊断行业扩容的最直接动力,2011年我国卫生机构的诊疗人次超过60亿人次,同比增速接近8%。2004年这一数字为40亿人次,7年间增加了超过20亿人次,我们认为未来我国人口的自然增速放缓,但是生活水平的提高和健康意识的加强将使诊疗人次稳步增长。
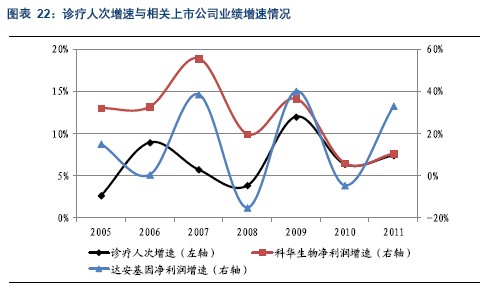
诊疗人次对体外诊断试剂生产企业的影响是显著而直接的,我们将2005年-2011年我国人诊疗人次增速与科华生物和达安基因的业绩增速进行对比,发现它们之间具有较好的吻合特征。
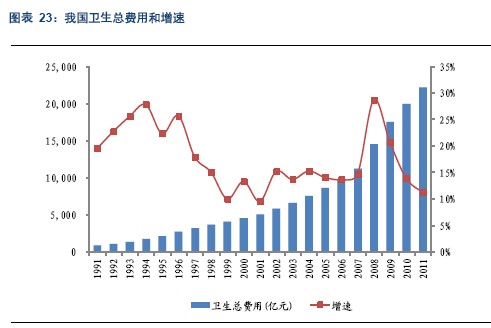
我们注意到我国的卫生总费用从2000年的4600亿元增长到2006年的接近1万亿用了大约6年时间;2010年我国卫生总费用接近2万亿元,比2006年又翻了一番,而这次翻番仅用了3年的时间。卫生费用规模的迅速扩张,一方面意味着医疗卫生市场的容量增大,另一方面我们也注意到,随着基数的增大,卫生费用的增速明显下降,2011年我国卫生总费用增速仅为11%左右,是历史低点。
我们认为未来体外诊断市场扩容的机会更多地蕴藏在卫生费用的内部调节中。目前的矛盾在于药品费用增长过快,药品费用在卫生总费用中的占比过高。
药品费用方面,2011年,我国的药品费用将近9400万元,同比增长了24%。2009年我国的药品费用大幅增长,随后三年都保持了较高的水平,而同期我国的医药卫生总费用增速已经出现了明显下滑。
药品费用占比方面,2008年药品费用在卫生总费用中的占比约为35%,是近十年的最低水平。但在之后,随着药品费用的大幅增长,药费在总费用的占比明显提升,2011年这一比例达到了42%。
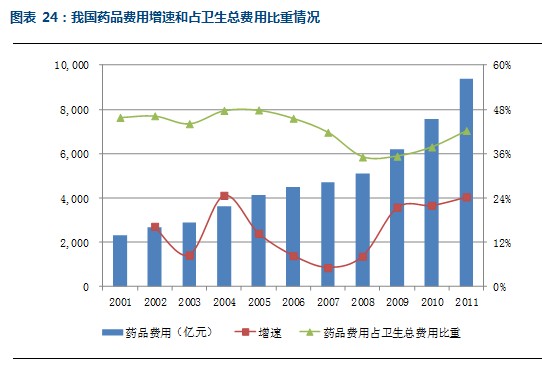
在医院收入和患者消费层面来看,根据卫生部公布的数据,2011年我国医院药品收入平均占总收入的44%,药品收入是公立医院的主要收入来源;同时在消费端,2011年门诊的次均消费中,药费占比超过55%,住院患者中,人均消费中超过40%用于药品消费。
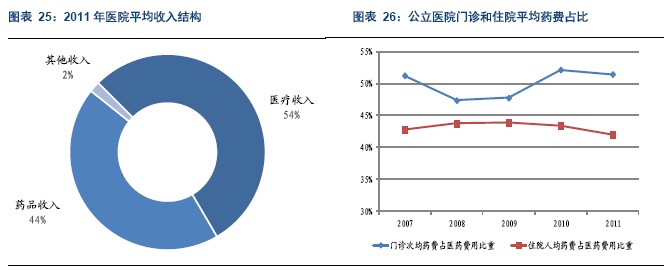
与主要发达国家相比,我国药费在总费用中的占比明显偏高。以2007年数据为例,美国的药费占比最低,仅为12%,占比最高的韩国也不过25%,而当年中国的比例为42%。药费占比下降将是未来我国卫生费用发展的趋势。
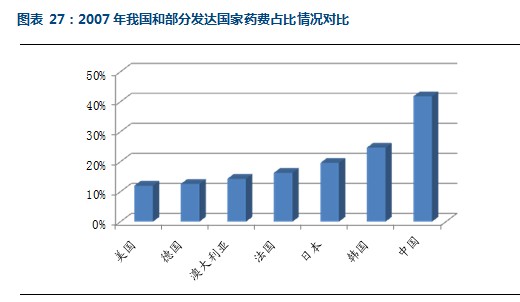
从政策层面方面来讲,国务院在今年四月公布的关于深化医药卫生体制改革2012年主要工作安排的通知中明确指出,未来改革的重点方向之一是调整医药价格,取消药品加成政策。提高诊疗费、手术费、护理费等医疗技术服务价格。体外诊断作为确定患者病症的重要手段,我们预计这项费用未来在总费用中的占比将有提升,这将成为未来体外诊断试剂和相关耗材市场扩容的重要来源之一。
4.2 传染病形势严峻,刺激诊断试剂行业发展
在我们前面提到的几大类诊断试剂中,免疫诊断试剂是占比最大的一类,约占全部诊断试剂的将近30%的市场份额,分子诊断占比相对较小,大约占4-5%的市场份额。免疫诊断试剂主要用于肝炎检测、艾滋病检测、肿瘤检测和孕检,分子诊断主要用于传染病的检测,它们未来将受益于国家对传染病大力控制而带来的市场扩容。
艾滋病发病人数逐年攀高
根据卫生部公布的数字,2000年我国艾滋病发病人数253人,而到了2011年这一数字已经上涨到20450人,11年增长了80倍;每十万人的发病率由0.02上升到1.53。
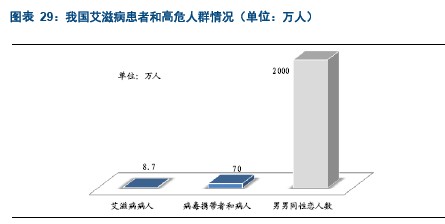
而这仅是艾滋病发病人数,由于艾滋病潜伏期较长,所以这个数字没有包括HIV病毒携带者数量,如果考虑病毒携带者,这一数字将更大。根据卫生部的统计年鉴,2000-2011年我国艾滋病发病人数总计在8.7万人左右,而根据卫生部公布的数据,2008年我国的艾滋病感染者和病人数量就已经达到了约70万人。
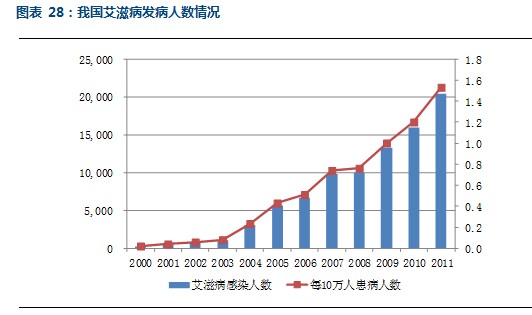
此外,我国艾滋病发病率上升的一个重要潜在威胁在于男男同性恋人数的上升。目前我国尚缺乏对该人群的准确统计,但是根据网易新闻转引青岛医学院张北川教授的观点,认为目前国内同妻(同性恋的妻子)数量在1000万以上,据此测算男性同性恋者数量至少在2000万上下。2006年由中国疾控中心牵头完成的首个国内男男同性恋调查报告显示,这一群体是艾滋病感染的高位人群,其感染率高达2.2-3.3%(不同城市见的差异),这一感染率是正常人群的1500倍以上。
国务院于2012年发布了《中国遏制与防治艾滋病“十二五”行动计划》(行动计划),根据该行动计划,我国将在2015年底,使艾滋病存活和感染者数量将控制在120万左右。
病毒性肝炎患者数量庞大
我国的病毒性肝炎患者患病率较高,2006年至今每10万人的患病人数稳定在100人左右。
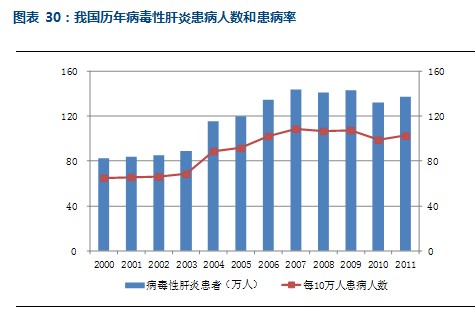
目前我国的乙肝病毒携带者数量估计超过1亿人,从卫生部公布的近几年我国每年检查出乙肝患者数量来看,总体上呈现出稳中有降的态势。我们认为这和近些年我国卫生部门开展的乙肝控制规划工作有关,根据我国对世界卫生组织的承诺,2012年我国的5岁以下乙肝病毒感染率控制在2%以下,而2006年我国的5岁以下儿童乙肝表面抗原携带率仅为0.96%。我们预计未来我国乙肝病毒携带者数量将继续保持稳中有降的趋势,但由于病毒携带者数量庞大,乙肝的控制形势依然严峻。
丙肝是病毒性肝炎中仅次于乙肝的第二大疾病,我们注意到丙肝患者数量增加显著。2008-2011年,我国乙肝患者数量总体下降,而丙肝患者数量的年均复合增速为17%,显著高于病毒性肝炎患者的整体增速。

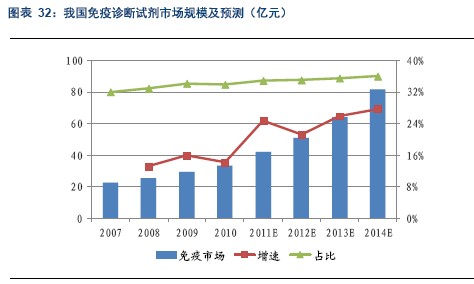
艾滋病和部分病毒性肝炎患病率的上升从一个侧面反映出我国传染病的防控面临着严峻形势,临床传染病检测目前主要使用的免疫诊断试剂,我们认为这将成为未来支撑免疫诊断发展的主要因素之一。预计2014年我国的免疫诊断试剂市场规模超过80亿元,市场占比小幅提升,达到36%左右。
4.3 血站系统核酸检测大力推广,或带来市场扩容
我们在上文中指出,体外诊断试剂行业的下游主要是临床检验和血源筛查,从总量和种类上来看,临床检验是最主要的消费端,血源筛查主要指血站系统,这一块的消费总量相对较小,诊断试剂使用范围也比较小,但是临床诊断的市场增量主要来自诊疗人次的提升,以及卫生费用的增长,而对于血站系统而言,血源筛查的核酸诊断试点工作正在进行,未来将全面铺开,将带动体外诊断试剂——尤其是核酸诊断试剂的市场规模的扩容。
血站系统的血液检测结果直接关乎临床用血的安全性,最终的检测结果是决定性信息,而临床的检测结果是给医生的参考性信息,所以血站系统对于诊断试剂的灵敏性要求要高于临床的诊断试剂。
目前我国有400多家血站,包括血液中心、中心血站和血站等等,先从献血量和献血人次上来看,1998年我国的采血量不到1000吨,献血人次不到250万人次,到2011年,采血量突破了4000吨,献血人次超过了1200万人次。献血人次的增加意味着血源筛查市场容量的扩大。
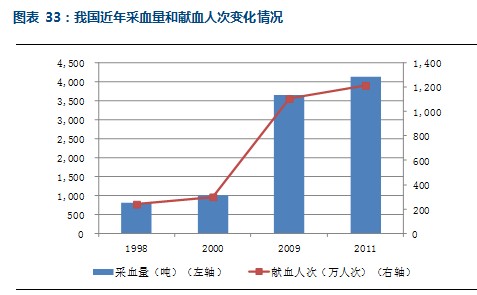
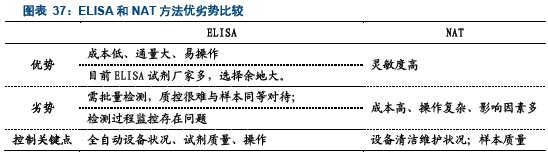
血站的血源筛查检测项目包括乙肝(HBV)、丙肝(HCV)、艾滋病(HIV)、梅毒、转氨酶(ALT)、血型、血红蛋白(Hb)、红细胞比容(HCT)和血小板计数(PLT)等。根据从今年6月1日开始执行的《血站技术操作规程(2012版)》,与2002年版本显著区别在于,对于乙肝(HBV)、丙肝(HCV)和艾滋病(HIV)的检测都增添了核酸检测的方法,而在2002年的规程中,这些项目的检测都使用的酶联免疫吸附测定法(ELISA)。
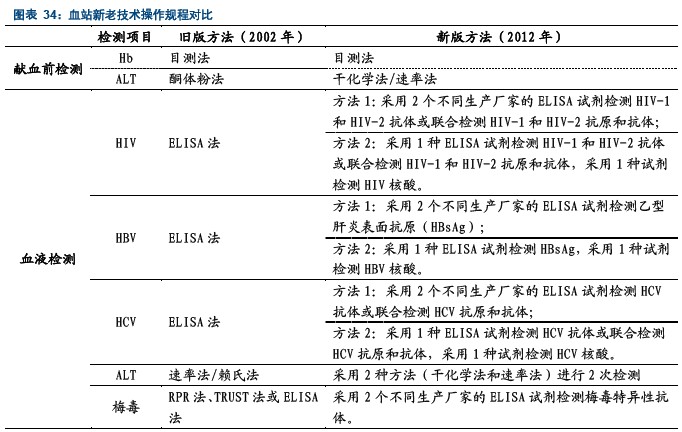
为何要开展核酸检测?核酸检测相比于ELISA检测,可以显著缩短窗口期,从而提高检测的准确性。下表中,黑色数字是ELISA检测方法的窗口期,红色数字是NAT方法的窗口期,通过对比我们可以发现,NAT方法的检测窗口期明显低于ELISA方法,换句话说,以HBV病毒检测为例,献血者如果在感染病毒的第17天献血,ELISA方法无法检测出来,应为该方法的窗口期为21天,而采用NAT方法就可以检测出阳性,因为该方法的窗口期为15天,提高了临床用血的安全性。
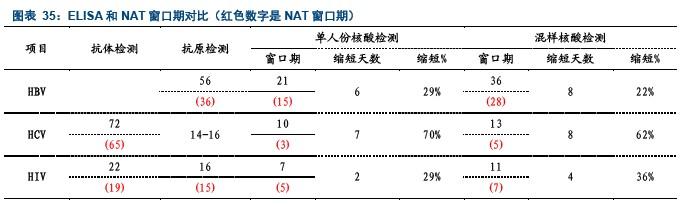
卫生部自2010年开始启动核酸检测(NAT)试点工作,一期共有15家血液中心参加。2010年3月至2011年12月,共完成核酸检测将近230万人份。根据我们的统计,在试点完成的这将近230万人份的核酸检测中,诺华和罗氏占据了将近80%的份额,国产试剂占比相对较小。正如我们前文所阐述的一样,血源筛查的检测试剂比临床检测试剂的灵敏度要求要高,目前进口产品在灵敏度和稳定性方面占有优势,所以诺华和罗氏的产品在NAT试点工作中占据了较大的份额。
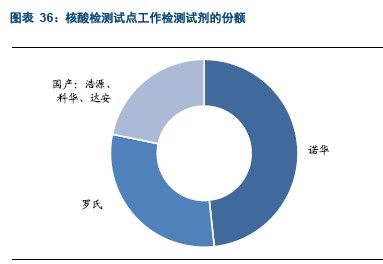
NAT方法与ELISA方法相比,最主要的优势是灵敏度高,这对于血站系统的血源筛查尤为重要,但是NAT方法的劣势在于其相对较高的成本、操作复杂和影响检测结果的因素较多。相比之下,ELISA方法虽然在灵敏度上逊于NAT方法,但是其成本低,可以实现高通量检测,并且操作简单,此外,ELISA试剂的选择余地也相对较多。这两种方法各有优势,根据《血站技术操作规程(2012版)》,未来的检测将是ELISA+NAT,它们不存在相互取代的关系。如果采用两种检测方法,那么从检测准确性角度考虑,两种方法不会选择同一品牌的诊断试剂。从目前试点推广的情况来看,诺华和罗氏占据了明显优势,但是我们认为未来NAT全面铺开后,国内厂商的市场份额将逐渐提高。科华生物、达安基因和浩源生物等公司将在这一领域占领自己的一块新阵地。
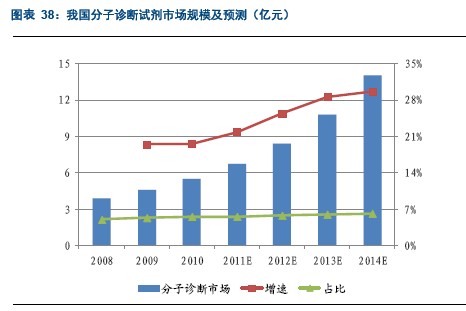
试剂行业中增速最高的一个细分领域。受益于我国未来对传染病控制的加强,血液筛查领域的核酸诊断推广,未来我国的分子诊断领域将实现高速的增长,预计2010-2014年的年均复合增速在26%以上。
4.4 行业整合,由分散走向集中
2005年全球前18名IVD企业占据了72%的市场份额,2007年前16家企业占据了76%的市场份额,而前四大IVD企业——罗氏、西门子、雅培、强生——占据了全球约一半的市场份额。

IVD行业的集中度在继续提升,尽管行业龙头企业已经占据了较大的市场份额,但是我们注意到,大型制药企业在不断地通过并购的方式实现集中度的进一步提升。2006-2007年西门子频繁出手,斥资超过150亿美元先后收购了DPC、拜耳(诊断)和德灵的诊断试剂业务,这也帮助西门子公司一跃成为全球第二大IVD生产企业。2009年贝克曼收购日本奥林巴斯诊断业务,时隔两年,贝克曼库尔特便被丹纳赫公司以68亿美元价格收购。作为IVD行业龙头的罗氏公司也没有停止收购扩张之路,2011年罗氏以1.19亿美元收购了德国PVT公司,进一步巩固了IVD行业龙头地位。

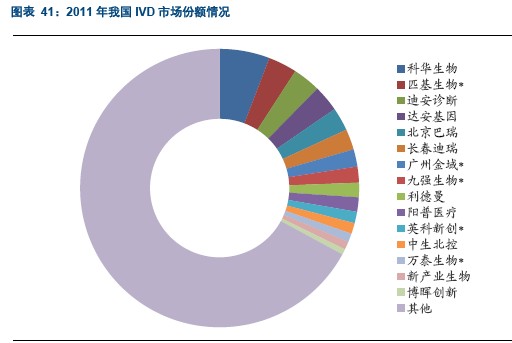
与我国医药行业的整体情况类似,我国IVD行业属于新兴产业,与欧美国家相比起步晚,产业化发展相对滞后。根据IVD专委会提供的数据显示,目前我国体外诊断试剂生产企业约300~400家,其中规模以上企业近200家,但年销售收入过亿元的企业仅约20家,企业普遍规模小、品种少。
我们对国内IVD市场情况进行了粗略统计,我们统计了国内IVD行业主要公司2011年的收入情况,经过我们粗略的统计,国内体外诊断行业的集中度明显偏低。科华生物、匹基生物和达安基因等15家IVD龙头企业,2011年收入之和仅占当年我国IVD市场规模的33%,而在前文中我们看到全球市场中,前5大企业就占据了全球50%以上的份额。我们认为我国IVD行业未来将通过并购实现行业集中度的提升,实力雄厚的医药企业也可能通过收购的方式进入IVD领域,例如人福医药计划通过非公开发行股票的方式收购北京巴瑞,从而进入IVD领域。